1、ヘルシンキ宣言と臨床試験実施の統一基準(世界医師会、World Medical Association)
...
1) 開発目標 |
|
|
|---|---|---|
2) 素材探し | 天然、合成 |
|
3)スクリーニングテスト |
|
|
4) 非臨床試験 |
| |
| a.毒性試験 1.単回投与毒性試験(急性毒性) 2種類以上の動物でLD50 2. 反復投与毒性試験 亜急性(3-7日) 3. 生殖発生毒性試験 4. 遺伝毒性(変異原性)試験 5. 癌原性試験 6. 抗原性試験 7. 局所刺激性試験 | 医薬品の安全性に関する非臨床試験の実施の基準 (Good Laboratory Practice、GLP)
|
| b.薬効薬理試験 1. 薬理作用 ED50、IC50 2. 安全性薬理試験 |
|
| c.薬物動態試験 1. 投与法、吸収 2. 分布 3. 代謝 4. 排泄 |
|
5) 臨床試験
| 二重盲検法 | |
a.第1相試験 | 少数健康男子、安全性、投与量、体内動態 | |
b.第2相試験 | 少数患者、安全性、有効性 | |
c.第3相試験 | 多数の患者、安全性、有効性 | |
6) 申請・審査 | 医薬品医機器総合機構 |
|
7) 生産・販売 |
| |
8) 第4相試験 | 長期安全性と有効性、市販直後調査6ヶ月間 | 市販後医薬品調査実施基準(Good Post-Marketing Surveillance Practice、GPMSP) |
9) 新薬の再審査 | 6~10年目に行う |
|
| 10) 再評価 | 5年間隔で有効性、安全性、品質の見直し |
...
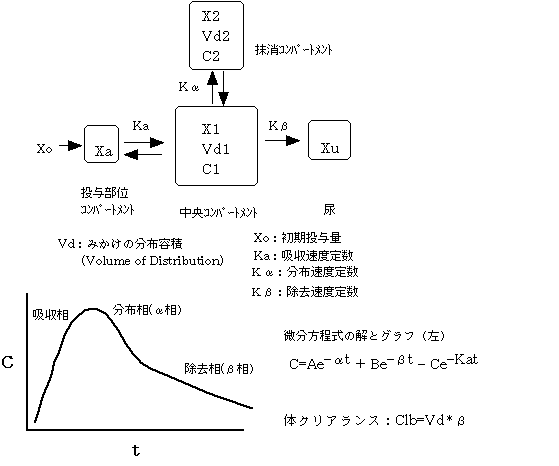
4)2分画モデル(two compartment model)註:以下の図の「抹消コンパートメント」は「末梢コンパートメント」の誤りです。
5)反復投与と薬物血中濃度
薬物を、静脈あるいは経口で反復投与する場合、投与間隔をその薬物の半減期にとると5回の投与により血中濃度は定常状態になり、血中濃度は初期ピークの2倍になる。点滴静注で持続的に投与する場合でも、その薬物の半減期の5倍の時間で定常状態になる。定常状態が有効血中濃度の範囲内にあることが重要である。もし、投与間隔を半減期の1/2にすると、初期ピークの3.4倍の血中濃度で定常状態になる。なお、薬物を間隔(τ)で投与した時の定常状態における平均血中濃(Cav)は、Cav=AUC/τで表される。
...
| 相互作用の生じる場所 | 組み合わせ例と相互作用 | その他 | |
|---|---|---|---|
| 吸収過程 | ・コレスチラミン(cholestyramine)(陰イオン交換樹脂、 胆汁酸吸着、高脂血症)により、酸性薬(ワルファリン(warfarin)、チアジド系、テトラサイクリン(tetracycline)、サイロキシン(thyroxine)、ジギタリス(digitalis))の吸収が阻害される。 | 吸着による吸収阻害 | |
| ・消化管運動作用薬のコリン系とドパミン系薬物 | 吸収の促進や抑制 | ||
| 分布過程 | ・アルブミンへの結合(ジギトキシン(digitoxin)、ワルファリン(warfarin)、ベンゾジアゼピン類など) ・α1酸性蛋白への結合(ジピリダモール(dipyridamole)、ジソピラミド(disopyramide)、キニジン(quinidine)、プロプラノロール(propranolol)など) | 血中の結合蛋白質に結合している薬物が、他の薬物と競合し、血中の遊離薬物濃度が上昇する。 | |
| 代謝過程 | |||
| i)肝マイクロソームの薬物代謝酵素系(CYP)の誘導 | ・ワルファリン(warfarin)(フェノバルビタール(phenobarbital)によるCYP2C9の誘導により、血液凝固の延長) ・経口避妊薬(リファンピシン(rifampincin)によるCYP2C19誘導による避妊失敗) | 喫煙、バルビツレート(barbiturate)、リファンピシン(rifampincin)、抗てんかん薬などがCYPを誘導する。 | |
| ii) CYP の阻害 | ・ケトコナゾール(ketoconazole)などの抗真菌薬によるCYP3A4阻害により、テルフェナジンの副作用の増強で、死に至る心室性不整脈が生じる。 ・ジヒドロピリジン系Caブロッカー(グレープフルーツの成分がCYP1A2を抑制し、作用増強)。 ・テオフィリン(theophylline)(ニューキノロンによるCYP1A2阻害による作用増強) | マクロライド系、キニジン(quinidine)、ニューキノロン類、サルファ剤、オメプラゾール(omeprazole)などが、CYPを阻害する。 | |
| iii)CYP以外の代謝拮抗 | ・5-FU(抗腫瘍薬)の毒性がソリブジン(抗ウイルス薬)により増強される。 | ソリブジンの代謝物により、5-FU分解酵素(ジヒドロピリミジンデヒドロゲナーゼ)が阻害される。 | |
| 排泄過程 | |||
| i)尿のpH変化による薬物再吸収の変動 | ・酸性尿(ビタミンC大量)で、酸性薬の排泄低下、塩基性薬の排泄増加 ・アルカリ尿(重曹、アセタゾラミド(acetazolamide))で、酸性薬の排泄増加、塩基性薬の排泄低下 | 酸性薬(アスピリン(aspirin)、フェノバルビタール(phenobarbital)、nalidixic acidなど) 塩基性薬(tetracyclin、イミプラミン(imipramine)、プロカイン(procaine)など) | |
| ii)有機アニオン分泌系の競合 | ・プロベネシド(probenecid)による、酸性薬(ペニシリン類、インドメタシン(indomethacin)、ワルファリン(warfarin)、経口糖尿病薬)の分泌抑制により、薬物濃度の上昇 | ||
| iii)有機カチオン分泌系の競合 | ・シメチジン(cimetidine)によるプロカインアミド(procainamide)の排泄抑制 | ||
| iv)P-糖蛋白質の競合 | ・キニジン(quinidine)によるジゴキシン(digoxin)分泌抑制 | ・イトラコナゾール(itraconazole)やベラパミル(verapamil)によるダビガトラン(dabigatran)血中濃度の上昇 | イトラコナゾールやベラパミルなどのP-糖蛋白質を強く阻害する医薬品を併用した場合、新規経口抗凝固薬のダビガトランのプロドラッグ体の吸収が亢進し、ダビガトランの血中濃度が上昇することが報告されており,抗凝固作用が増強され、大出血を起こす可能性がある。イトラコナゾールの経口製剤は,特に強い阻害作用を示すため,ダビガトランと併用禁忌となっている。 |
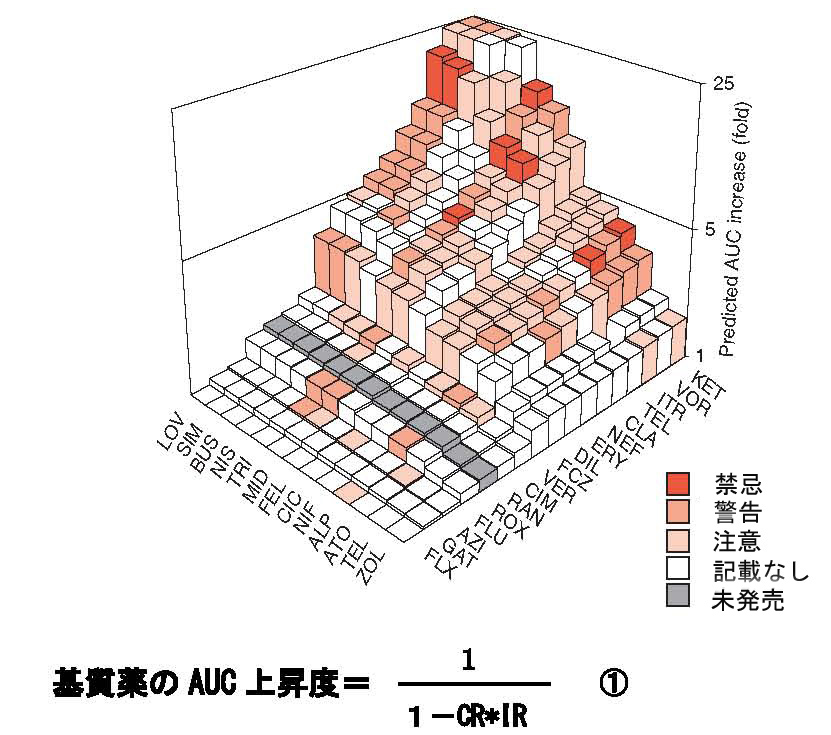
| CYP3A4の基質薬と阻害薬の相互作用による基質薬の血中濃度予測と、添付書類(米国)での警告 阻害薬(inhibitor)を併用したときの基質薬(substrate)のAUCを求めると、①式の関係が成立する。もしIR(inhibition ratio)とAUCが分かれば、CR(contribution ratio)が求められる。例えば、基質薬SIMを、阻害薬CLA(IRは0.88)と併用して、AUCを実測したとき、AUCの増加が8.3倍であれば、CRは1.0と計算される。上のグラフは、さまざまなCYP3A4の基質薬と阻害薬を併用したときのAUC増加倍数を予測したものである。添付書類(米国)で、薬物相互作用の警告が記載されている組み合わせは赤色の濃淡で示されいる。わが国の添付書類での警告記載は米国の58%である。 (図と説明は、A.Hisaka et al, Clin. Pharmacokinet. 48, 653, 2009より引用) 阻害薬(右から活性の強い順): ケトコナゾール(ketoconazole、KET), voriconazole (VOR), イトラコナゾール(itraconazole、ITR), telithromycin (TEL), クラリスロマイシン(clarithromycin、CLA), nefazodone (NEF), エリスロマイシン(erythromycin、ERY), ジルチアゼム(diltiazem、DIL), フルコナゾール(fluconazole、FCZ), ベラパミル(verapamil、VER), シメチジン(cimetidine、CIM), ラニチジン(ranitidine、RAN), roxithromycin (ROX), フルボキサミン(fluvoxamine、FLU), azithromycin (AZI), gatifloxacin (GAT) and fluoxetine (FLX). 基質薬(左から阻害薬に感受性の強い順): lovastatin (LOV), シンバスタチン(simvastatin、SIM), buspirone (BUS), nisoldipine (NIS), トリアゾラム(triazolam、TRI), midazolam (MID), felodipine (FEL), シクロスポリン(ciclosporin、CIC), ニフェジピン(nifedipine、NIF), alprazolam (ALP), アトルバスタチン(atorvastatin、ATO), telithromycin (TEL), and ゾルピデム(zolpidem、ZOL). |
...