解熱鎮痛薬・抗炎症薬(Anti-inflammatory Drugs)
1、疼痛発現機構
痛みを誘発する刺激は組織の損傷をひきおこすので、侵害刺激(noxious stimulus)という。
侵害刺激→組織障害→発痛物質(bradykinin、prostaglandins, serotonin, histamineなど)→自由神経終末→→痛覚伝導路
TRP(transient receptor potential)チャネルと痛みについて
TRPチャネルは6回の膜貫通領域を有する陽イオンチャネルで、大きなスーパーファミリーを形成している。その中の1つカプサイシン(唐辛子の成分)受容体TRPV1は、感覚神経特異的に発現し、カプサイシンだけでなくプロトン、熱などによっても活性化される多刺激痛み受容体として機能することが知られている。さらに、ブラジキニンなどの炎症関連メディエイターはPKCを介して、プロスタグランジンはPKAを介してTRPV1の機能に影響すると考えられている。
2、発熱機構
視床下部の体温調節中枢がサーモスタットの役割をしている。
外因性発熱物質(endotoxinなど)→白血球やマクロファージへの取り込み→内因性発熱物質(interleukin-1など)の産生→PGE2→サーモスタットの高温設定→発熱
3、炎症発現機構
炎症性刺激(火傷、外傷、細菌感染、抗原抗体反応など)→血管透過性亢進期(histamine, PGsなどのchemical mediatorsの遊離による紅潮や熱感)→白血球遊走期(白血球の遊走や血小板の凝集による疼痛や腫脹)→細胞増殖期(単球の浸潤、肉芽形成、血管新生)→治癒あるいは慢性化
4、Chemical mediatorsについて
炎症反応は、血管系の反応、細胞遊走、細胞増殖などの様々な反応が複雑に関与している。これには化学伝達物質(chemical mediators)が仲介反応をしている。
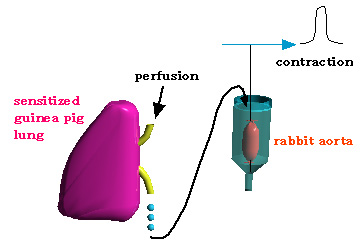
chemical mediators発見の歴史的実験を以下に示す。
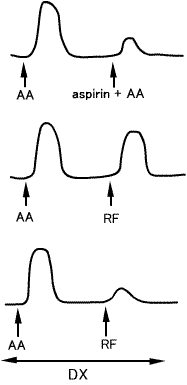
(左or 上図)感作したモルモットの肺を摘出し、灌流する。このとき抗原を加えると、ウサギ大動脈を収縮させる物質(RCS, rabbit aorta contracting substances)が出てくる。RCSは、RCS-releasing factor(RF), histamine, 5-HT, bradykininなどが主成分である。 |
5、抗炎症薬(Anti-inflammatory drugs)
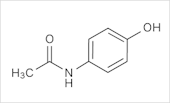
A) 非ステロイド性抗炎症薬(non-steroidal anti-inflammatory drugs 、NSAIDs)とアセトアミノフェン(acetaminophen)
構造式はさまざまであるが、解熱、鎮痛、抗炎症の共通作用を持つ。体性痛に有効であるが、内臓痛にはほとんど効かない。抗炎症作用の強さは薬物により大きく異なる。NSAIDsはアラキドン酸の代謝経路のシクロオキシゲナーゼ(COX)を阻害することで、プロスタグランジン類(prostaglandins)の合成を抑制する(下図)。プロスタグランジン類の中では、特にプロスタグランジンE2(PGE2)が起炎・発痛増強に関与すると考えられている。アセトアミノフェン(acetaminophen)は鎮痛・解熱作用を有するが、抗炎症作用はほとんどない。このためアセトアミノフェンはNSAIDsには分類されない。作用機序は、中枢神経系におけるCOX阻害と考えられているが、詳細な機序は不明である。
COXには、COX-1とCOX-2というアイソザイムがあり、COX-2は炎症刺激により発現が誘導される。COX-1は構成的に発現している。NSAIDsの主な副作用である胃腸障害は、胃粘膜におけるCOX-1阻害によって粘膜細胞保護効果をもつPGI2、PGE2などの減少によると考えられている。特異的COX-2阻害薬(セレコキシブ、メロキシカムなど)以外のNSAIDsはCOX-1とCOX-2の両方を阻害する。
非ステロイド性抗炎症薬の分類 | 非ステロイド性抗炎症薬 | 薬理作用および副作用 |
|---|---|---|
サリチル酸 | アスピリン(aspirin) | 下記に記載。 |
インドール酸誘導体 | インドメタシン(indomethacin) | 下記に記載。 |
スリンダク(sulindac) | プロドラッグ(prodrug)であり、体内で還元されて作用する。 | |
ピラゾロン誘導体 | スルピリン(sulpyrine) | 古くより用いられているピリン系解熱・鎮痛薬であるが、過敏症などのために使用頻度は減少している。 |
プロピオン酸 | イブプロフェン(ibuprofen) | 慢性関節リウマチなどに抗炎症薬として用いられる。胃腸障害などの副作用が少ない。cyclooxygenaseの阻害は可逆的である。 |
ナプロキセン(naproxen) | ibuprofenと同じ | |
ケトプロフェン(ketoprofen) | 解熱作用が強い。 | |
| ロキソプロフェン(loxoprofen) | プロドラッグのため胃腸障害が比較的少ないとされている。国内開発のため日本では最も頻用されているNSAIDであるが米国FDAは承認していない。 | |
フェナム酸誘導体 | メフェナム酸(mefenamic acid) | 鎮痛作用が強い。激しい下痢を引き起こすことがある。インフルエンザ感染の小児には禁忌。 |
フルフェナム酸(flufenamic acid) | 鎮痛作用が強い | |
ヘテロアリル酢酸誘導体 | ジクロフェナク(diclofenac) | COX阻害はindomethacinより強い。慢性炎症に対して有効。インフルエンザ脳炎・脳症には禁忌。 |
フェンブフェン(fenbufen) | プロドラッグであるので、胃腸障害は少ないと考えられる。 | |
チアジン誘導体 | ピロキシカム(piroxicam) | indomethacinとほぼ同じCOX阻害作用を持つ。 |
塩基性抗炎症薬 | チアラミド(tiaramide) | COX阻害作用はほとんどないが、鎮痛・解熱・抗炎症作用を示す。 |
特異的COX-2阻害薬 | セレコキシブ(celecoxib) | COX-2を選択的阻害することにより、COX-1 阻害で引き起こされる胃腸障害がほとんど生じない。他の作用は、NSAIDsとほとんど同じである。関節リウマチに用いられる。長期投与で、心筋梗塞と脳梗塞のリスクがある。IC50比を比較すると、celecoxib: COX-1/COX-2=375/1、アスピリン(aspirin): COX-1/COX-2=0.006/1 である。 |
パラアミノフェノール誘導体 | アセトアミノフェン(acetaminophen) | 解熱・鎮痛作用を持つ。抗炎症作用は弱い。ライ症候群(Rey's syndrome)を引き起こさないので、ウイルス感染の小児の解熱にはasprinよりも優れている。胃腸障害は少ない。過剰投与で重篤な肝障害をきたす。これは、肝臓でのP450で少量の反応性の高いN-水酸化代謝物ができ、glutathioneと反応するが、glutathioneがなくなると、毒性が出るため。 |
妊娠時のNSAIDSについて
妊娠に対してはいずれのNSAIDSも使用をなるべく避けた方が無難である。胎児への催奇形性の指摘は特にないが、妊娠後期に使用すると胎児動脈管の早期閉鎖を促すことがある。それゆえ、NSAIDSよりもアセトアミノフェンの安全性が高い。また、妊娠中の関節リウマチなどの強い炎症・疼痛のコントロールには低用量ステロイドが安全である。
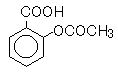
1) アセチルサリチル酸(acetylsalicylic acid 、aspirin)
ヤナギの皮からのsalicinが発熱に有効であることが知られていた。salicinの水解により、glucose、salicylateができる。1875年 Bussがsodium salicylateを合成、1899年 Nenckiがアスピリン(aspirin)を合成した。
薬理作用 | 解説 |
|---|---|
鎮痛作用 | シクロオキシゲナーゼ(cyclooxygenase、COX)を不可逆的に阻害することにより、PGE2とPGI2を産生抑制し、末梢性に鎮痛効果をしめす。 |
解熱作用 | 体温調節中枢におけるPGE2産生抑制により解熱をきたす。正常体温は下げない。 |
抗炎症・抗リウマチ作用 | 鎮痛作用の5倍の血中濃度が必要。カリクレイン(kallikrein)系のchemical mediatorsを抑制するので、顆粒細胞の障害血管への付着抑制や、lysosomeの安定化作用。白血球の遊走を阻害する。 |
血小板凝固抑制 | TXA2の産生抑制により、血小板凝集を抑制する。この効果は8日以上持続する。冠動脈硬化や心筋梗塞の予防効果がある。 |
尿酸排泄作用 | 腎尿細管からの尿酸の分泌を促進する。 |
呼吸 | 直接、間接的に呼吸を刺激する。酸素消費上昇、呼吸中枢刺激によりrespiratory alkalosisを起こす。 |
酸塩基平衡 | 治療量でrespitratory alkalosisを起こすが、腎での(bicarbonateの排泄増)により代償される。中毒量では、子供において、血液pHの低下(bicarbonateの減少による)とrespiratory およびmetabolic acidosisを引き起こす。 |
アスピリン(aspirin)
アスピリン(aspirin)は、COX-1とCOX-2の両方を阻害するが、COX-1をより強く阻害する。COX-1のSer-530をacetyl化することにより非可逆的に活性を阻害する。 |
副作用 | 解説 |
|---|---|
胃粘膜出血・胃潰瘍 | PGE2およびPGI2産生を抑えると胃粘膜の虚血、胃酸分泌の亢進、粘膜保護作用の障害などを引き起こす。 |
薬物アレルギー | 喘息、鼻炎、発疹など。(fenamicやsulindacでは5-10%に出現する) |
ライ症候群(Rey's syndrome) | ウイルス性発熱の小児に用いると、Rey's 症候群(脂肪肝を伴う脳症)を引き起こすことがある。小児の解熱にはアセトアミノフェンが推奨される。 |
中枢神経系 | 大量投与で、頭痛、めまい、耳鳴り、呼吸性アルカローシスなどが生じる。 |
腎毒性 | PGE2およびPGI2は、腎血管の拡張作用があり、腎血流量を調節しているので、asprinにより、腎障害を引き起こす。 |
| アスピリン喘息 | アスピリン喘息はNSAIDsによって誘発される喘息をいう(アスピリンに対してだけではない)。喘息患者の約10%に認められる (救急外来で頻繁に問題となる)。ときに、意識障害をきたすほどの大発作となり、死にいたることもある。COX 阻害活性の弱いものの方が、危険性は少ないとされている (アセトアミノフェンや塩基性消炎剤の方が、起きる頻度は少ないとされている。)ロイコトリエン拮抗薬の併用によって、喘息コントロールが有意に改善される。COX阻害によってロイコトリエンが増加することで発症すると考えられている。 |
アスピリンとがん、アスピリンとアルツハイマー病
梗塞予防で服用する患者を用いた臨床研究からアスピリンが発がん(特に大腸がんなど)予防に有効であることはほぼ確立した。一方、アルツハイマー病についての有効性については現在のところ否定的である。
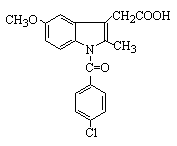
2)インドメタシン(indomethacin)
強力なCOX阻害薬であり、強い解熱鎮痛・抗炎症作用を持つ。アスピリン(aspirin)よりも胃腸障害の頻度は高い。長期連用により角膜混濁がでる。多核白血球の遊走を抑制する。35-50%に副作用あり。
indomethacin
3)アセトアミノフェン(acetaminophen)
アセトアミノフェン(acetaminophen)は鎮痛・解熱作用を有するが、抗炎症作用はほとんどない。このためアセトアミノフェンはNSAIDsには分類されない。作用機序は、中枢神経系におけるCOX-3阻害と考えられていたが、その後の研究でCOX-3阻害作用と臨床効果の相関が弱いことがわかった。アセトアミノフェンは肝臓でp-アミノフェノールへ代謝され、、このp-アミノフェノールが脳内へと移行し、脂肪酸アミド加水分解酵素によってアラキドン酸と結合したN-アラキドノイルアミノフェノール(AM404)へと変わることで、鎮痛作用を示すという説が現在では有力となっている(2023年9月の時点)。
比較的安全性の高い薬物であり、オピオイドとの併用で作用が増強する。単独使用による消化管障害は少ない。最も重要な副作用は肝障害であり、用量依存的に肝障害リスクは増大する。特に、肝機能の低下している高齢者での使用には注意が必要である。重症の肝毒性に対してはアセチルシステインを投与する。
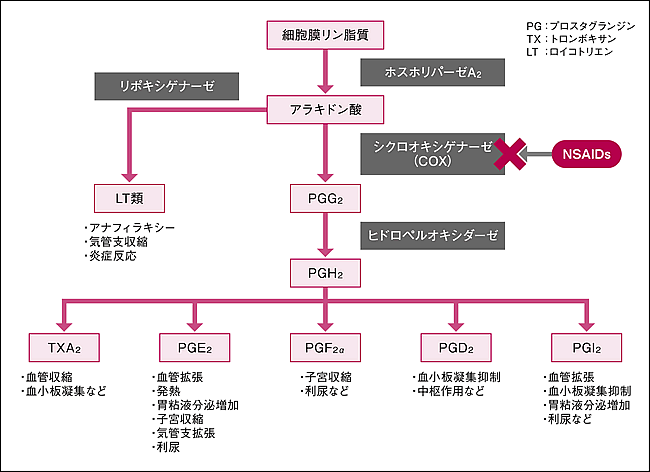
アラキドン酸の代謝経路(arachidonic acid cascade)とNSAIDsの作用部位
(日本緩和医療学会のサイトより転載)
B) ステロイド性抗炎症薬(Steroidal anti-inflammatory drugs)
1)薬物
薬物 | 錠剤中の量(mg) | 半減期 | 抗炎症作用 | ナトリウム貯留作用 (ミネラルコルチコイド作用) |
|---|---|---|---|---|
ヒドロコルチゾン(hydrocortisone、コルチゾール (cortisol)) | 10 | 短 | 1 | 1 |
| コルチゾン(cortisone) | 25 | 短 | 0. | 0.8 |
プレドニゾロン(prednisolone) | 5 | 中 | 4 | 0.8 |
メチルプレドニゾロン(methylprednisolone) | 4 | 中 | 5 | 0.5 |
トリアムシノロン(triamcinolone) | 4 | 中 | 5 | 0 |
| デキサメタゾン(dexamethazone) | 0.5 | 長 | 25 | 0 |
ベタメタゾン(betamethazone) | 0.5 | 長 | 25 | 0 |
成人hydrocortisoneの分泌量は、20mg/日 とされてきたが、近年の研究で約10mg/日と修正されている。上記の基本となる錠剤の通常1錠中には、成人副腎1日分泌量相当ないし約2倍量を含んでいることになる。それぞれの薬剤と、副腎萎縮の副作用の出現頻度の関係を押さえておくこと。
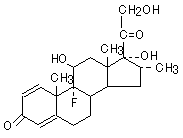
デキサメタゾン(dexamethazone)
2)グルココルチコイド(glucocorticoid)の薬理作用
薬理作用 | 解説 |
|---|---|
糖新生の増加 | 血糖値上昇、糖尿病 |
末梢での糖利用減少 | 血糖値上昇、糖尿病 |
脂肪代謝 | 脂肪沈着、中心性肥満 |
蛋白異化作用の増加 | 筋消耗、小児の成長抑制 |
電解質代謝 | 血清K低下、血清Na上昇 |
炎症反応の低下 | 抗体産生低下、細胞性免疫低下、易感染性 |
骨異化作用 | 骨粗鬆症 |
精神変調 |
|
3)臨床適応と注意点
副腎ステロイドのよる治療は、ホルモン分泌不全による補充療法以外は、抗炎症作用と免疫抑制作用を目的として用いられることがほとんどで、あくまでも対症療法であり、原因療法ではない。抗炎症作用発現には、mRNA合成、タンパク質合成が必要であり、少なくとも 1-2 時間が必要である。
突発性血小板減少性紫斑病、ネフローゼ症候群、気管支喘息発作重積状態、慢性関節リウマチ、白血病などの、アレルギー性疾患、膠原病や悪性腫瘍などに広く用いられる。glucocorticoidの必要量は、抗体産生抑制作用は、抗炎症作用に比べれば多量のステロイドが必要である。
長期投与の場合は、有効最少量を使用する。副腎ステロイドを急に中止すると、①従来からあった疾患の症状が悪化する反跳現象(rebound phenomenon) 、②副腎皮質機能不全を起こす離脱症候群(withdrawal syndrome) が現れる。使用量を少しずつ減少させる漸減法(tapering) により、他の薬で置換するように工夫する。
withdrawal syndromeは、一日のステロイド分泌量をこえる量を長期使用していた場合(例えば2週間以上)に起きやすいと言われている。発熱、筋肉痛、関節痛、食欲不振、悪心、ショックなどを引き起こす。
アンテドラッグ(antedrug):投与部位では活性を有し、体内に入ると速やかに代謝されて不活化するか、または活性が低くなる。全身的副作用を軽減する目的で開発された薬剤。プロドラッグとは逆の機構のもので、鼻アレルギー、気管支喘息などに使われ、副作用軽減の観点から重要である。
リファンピシン (抗結核薬)などのCYP3A4を誘導する薬剤との併用によって、ステロイドの代謝が亢進する。デキサメタゾンやベタメタゾンは特に影響を受け易いので、併用する場合はこれらのステロイドを増量する必要がある。。CYP3A4を誘導する薬剤としては他に、フェニトイン (抗てんかん薬)、フェノバルビタール (抗てんかん薬)、カルバマゼピン (抗てんかん薬)などがある。
4)グルココルチコイド(glucocorticoid)の副作用
副作用 | 解説 |
|---|---|
感染症の増悪や誘発 | 感染に対する血管の反応、白血球やマクロファージの機能低下、抗体産生抑制などによる。 |
消化性潰瘍 | 多量のglucocorticoidの治療でよく見られる。 |
糖尿病・高血糖 | 多量のglucocorticoidの治療でよく見られる。 |
血栓、動脈硬化、血管炎 |
|
精神症状 | 長期のsteroid治療で見られる。多幸感、不眠症、不安感など。 |
骨折 | 蛋白異化作用での筋肉の弱化、骨粗鬆症による。 |
副腎不全 | ACTHの分泌抑制による。 |
ニキビ |
|
多毛症 |
|
骨粗鬆症 |
|
満月様顔貌 | 脂肪代謝異常による。 |
体重増加 |
|
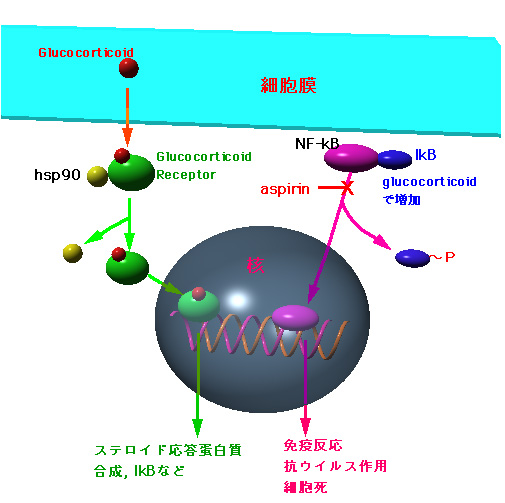
5)glucocorticoidの作用機序
glucocorticoidsの作用機序 |
6、関節リウマチ治療薬(抗リウマチ薬、Antirheumatic drugs)
関節リウマチ(RA)は、関節を包んでいる滑膜の炎症が引き金になり、リンパ球や白血球などの免疫細胞が浸潤し、次第に滑膜から軟骨、骨へと炎症が波及し、やがて関節自体を破壊する疾患である。原因は不明であるが、遺伝的素因やウイルスなどの感染症が絡んだ自己免疫疾患と考えられている。罹患率は人口の0.8%で、全ての年齢に発生する。女性に多く(男:女=1:3)、40歳代に発生のピークがある。
抗リウマチ薬は、疾患修飾抗リウマチ薬(DMARDs、disease-modifying antirheumatic drugs)とも呼ばれる。抗リウマチ薬は免疫調節薬、免疫抑制薬、生物学的製剤の3つに分類される。
「関節リウマチ治療におけるメトトレキサート(MTX)診療ガイドライン2011年版」によると、「関節リウマチと診断されて予後不良と思われる患者では,リスク・ベネフィットバランスに鑑みて,MTXを第1選択薬として考慮する。他の低分子経口抗リウマチ薬(低分子DMARDs)の通常量を2-3カ月以上継続投与しても、治療目標に達しないRA患者には積極的にMTXの投与を考慮する。」と記されている。
近年の生物学的製剤やJAK阻害薬の開発によって、リウマチ治療は大きく進歩し、リウマチ患者全体の約3分の2が寛解もしくは低活動性の状態にできるとされている。今後は、残り3分の1の高疾患活動性の制御が課題である。
分類 | 薬物 | 作用点および副作用 | |
|---|---|---|---|
抗リウマチ薬 |
| 作用発現に1~3ヶ月かかる。 | |
| 免疫調節薬 | 1) ブシラミン(bucillamine) | 1) サプレッサ-T細胞比を増加させ、免疫グロブリンやリウマトイド因子活性を低下させる。D-penicillamineと作用は同じ。 |
免疫抑制薬 | 1) メトトレキサート(methotrexate、MTX) | 1) DNA合成阻害により、リンパ急増直抑制。有効性が明確で、第一選択薬。生物学的製剤と併用される。副作用:過敏症、間質性肺炎、肝障害、腎障害。 | |
| ヤヌスキナーゼ(JAK)阻害薬 | 1) トファシチニブ(tofacitinib) | 1)JAK(1と3)阻害。JAK3を阻害することで、IL-2、15、17の抑制と樹状細胞の活性化、B細胞の抗体産生を抑制するとされる。適応はメトトレキサート (MTX) で効果不十分または効果が見られない 中等度から重度の関節リウマチ。 2)JAK(1と2)阻害。JAK3は阻害しない。JAK2に選択的に結合する事でGM-CSF、IL-6、IFNγの産生を抑制するとされている。 | |
生物学的製剤 | 1) インフリキシマブ(infliximab) | 炎症性サイトカインを抑制する効果発現が早く、RA病変が完全寛解することもある。分子量が大きく、経口投与できない。 1)TNFαを阻害するモノクローナル抗体、IL-6の産生抑制やTNFα産生細胞の傷害を引き起こす。副作用:結核、敗血症などの感染症、Infusion reaction、過敏症。 2) 可溶性TNFα受容体。デコイ受容体として腫瘍壊死因子TNF-αとTNF-βの両方に結合し、TNF受容体へのシグナル伝達を阻害する。 3) 完全ヒト抗TNFαモノクローナル抗体。TNFαの作用を阻害。 4) ヒト化抗IL-6受容体抗体。IL-6の作用を阻害。 | |
ステロイド | プレドニゾロン(predonisolone)など | Steroidsの項目参照 | |
NSAIDs | メロキシカム(meloxicam) | NSAIDsの項目参照 | |
関節破壊の進行を遅らせる効果が証明されている薬物は上記のDMARDsのうち、サラゾスルファピリジン(salazosulfapyridin)、 メトトレキサート(MTX)、レフルノミド(leflunomide)、インフリキシマブ (MTX併用)、 エタネルセプト(etanercept)、アダリムマブ(adalimumab)、トシリズマブ(tocilizumab)である。
関連サイトの紹介
1、日本緩和医療学会 がん疼痛の薬物療法に関するガイドライン 薬理学的知識 非ステロイド性消炎鎮痛薬(NSAIDs)
2、日本ペインクリニック学会 NSAIDsとアセトアミノフェン
3、メディカルノート アスピリン喘息(別名:NSAIDs過敏喘息/解熱鎮痛薬喘息)
4、大阪大学大学院医学系研究科 呼吸器・免疫内科学 ステロイドについて
5、Mapionニュース 2021年のノーベル生理学・医学賞は「温度と触覚の受容体」の発見者
(久野、三木)