統合失調症治療薬(Drugs for Schizophrenia and Related Disorders)
統合失調症(精神分裂病)は、人口の約1%に見られ、多くは青年期に発症し、妄想、幻覚のほか、自我や感情障害などを主症状とし、再燃と寛解を繰り返す。
1、統合失調症には、Bleulerの4Aといわれる基本症状がある
1) Association | 観念連合の弛緩、分裂思考 |
2) Affect | 感情障害 |
3) Ambivalence | 両価性 |
4) Autism | 自閉 |
2、Schneiderの第1級症状が診断に用いられる
考想化声、対話幻聴、注釈幻聴、批評幻聴、身体被影響体験、 思考奪取、思考干渉、思考伝搬、思考注入、妄想知覚、感情・欲動・意志の作為体験と被影響体験
3、症状は、大きく陽性症状と陰性症状に分けられる
陽性症状 | 精神運動興奮で、いらいら、不眠、不安、幻覚、妄想、思考滅裂など |
陰性症状 | 意欲喪失、自発性欠如、人嫌い、自閉、感情鈍麻など |
4、統合失調症の脳内変化として次のような知見がある
A.神経系の発達障害 | 1)前頭部低活性(hypofrontality)PETやSPECTで、前頭葉の血流低下が見られ、陰性症状と相関する。 |
|---|---|
B.ドパミン(Dopamine、DA)系の異常(DA過剰説) | D4受容体の増加、D1受容体の減少。シナプス間隙のDAレベルが高い。また、DAによるD2受容体の占有率も高く、これが陽性症状と相関する。D2受容体のミスセンス変異などが報告されている。 |
C.グルタミン酸系の異常 | NMDA受容体の機能障害がある。PCP(NMDA受容体阻害薬)が妄想・幻覚を引き起こす。 |
D.セロトニン系の異常 | 5-HT2阻害薬のクロザピン(clozapine)やリスペリドン(risperidone)が陰性症状に対して有効である。5-HT2A mRNAが統合失調症の前脳皮質で低下している。LSDやpsilocibinなどが幻覚を引き起こす。DA過剰説のみでは陰性症状の説明ができない。 |
E.脳内キヌレン酸の異常 | トリプトファン代謝物のキヌレン酸が増加している。キヌレン酸はグルタミン受容体を遮断する。 |
F.遺伝子解析 | 一卵性双生児の統合失調症発症の一致率は約70%と高いことから遺伝的素因の関与が強く疑われてきたが、現在では、広範な標的遺伝子群のどれかに新しい機能破壊変異が生じた場合に、統合失調症という症状が現われるという多標的遺伝子仮説が有力である。 |
5、統合失調症の治療薬
1950年代初頭に統合失調症の治療薬として、2つの画期的な治療薬が発見された。クロルプロマジン(chlorpromazine)とレセルピン(reserpine)である。1952年にクロルプロマジンの効果が示されて以来、フェノチアジン系、ついでブチロフェノン系の定型薬とよばれる薬物が開発された。これらは錐体外路症状、遅発性ジスキネジア、悪性症候群など副作用が著明であった。現在では、これらの副作用が少ないリスペリドンなどの非定型薬とよばれる薬物が多く用いられている。
6、治療薬の分類
現在のところ、原因を治療できる薬物はなく、全て対症療法として用いられる。
第1世代薬(定型薬) | 高力価群 | 低力価群 | 中間・異型群 |
|---|---|---|---|
D2遮断作用が強い。錐体外路症状がでやすい。鎮静・循環系の副作用が少ない。 | 鎮静作用が強い。錐体外路症状がでにくい。自律神経や循環系の副作用が出やすい。 | 鎮静作用や錐体外路症状は軽い。賦活作用がある。 | |
フェノチアジン(phenothiazine)系 | フルフェナジン(fluphenazine) | クロルプロマジン(chlorpromazine) | プロペリシアジン(propericiazine) |
ブチロフェノン(butyrophenone)系 | ハロペリドール(haloperidol)、スピペロン(spiperone) | フロロピパミド(floropipamide) | モペロン(moperone) |
イミノジベンジル(iminodibenzyl)系 | カルピプラミン(carpipramine) | ||
ベンズアミド(benzamide)系 | スルピリド(sulpiride) |
第2世代薬(非定型薬) | 治療効果は中程度。陽性症状と陰性症状の両方に有効。錐体外路症状の副作用が出にくい。 |
|---|---|
セロトニン・ドパミン遮断薬(SDA、serotonin-dopamine antagonist) | セロトニンとドパミンが錐体外路系で拮抗することを利用して、中脳‐辺縁系のドパミン神経を遮断しながら、セロトニン受容体も遮断することで錐体外路症状が少ないといわれている。漏斗‐下垂体系のドパミン神経は遮断するので、高プロラクチン血症や乳汁分泌をおこすことがある。 |
| リスペリドン(risperidone (serotonin-dopamin antagonist, SDA))、陽性症状に良く用いられる。 | |
| ペロスピロン(perospirone (serotonin-dopamin antagonist, SDA)) | |
| ブロナンセリン(blonanserin) | |
| 多元受容体作用抗精神病薬(MARTA、multi-acting-receptor-targeted-antipsychotics) | ドパミンD2受容体群(D2、D3、D4)、5-HT2受容体、5-HT6受容体、アドレナリンα1、ヒスタミンH1受容体など多くの神経伝達物質受容体を遮断する。錐体外路症状をおこしにくいといわれている。 |
クロザピン(clozapine) | |
オランザピン(olanzapine)、陽性症状に良く用いられる。 | |
| クエチアピン(quetiapine) | |
ドパミン部分アゴニスト(DA partial agonist) | シナプス後D2の弱い遮断作用だけでなく、シナプス前D2(自己受容体)の刺激作用(partial agonist)として働く 。ドーパミン神経系の過活動では抑制し、低活動では活性化することでドーパミン神経系を安定化するといわれている。錐体外路症状や乳汁分泌などの副作用が少ない。 |
アリピプラゾール(aripiprazole)、陰性症状に良く用いられる。顕著な症状のない患者の再発予防に対する第1選択薬としても用いられる。 |
第1世代のD2受容体遮断薬(定型、typical)は、陽性症状に効くが、陰性症状に効き難く、また錐体外路症状などの副 作用がでる。しかし、第2世代(非定型薬、atypical)は、D2受容体遮断よりも、5-HT2A受容体遮断作用が強く、陰性症状の改善や、錐体外路症状の副作用が少ないのが特徴である。SerotoninはDAの遊離を抑制している。5-HT2A受容体遮断は、黒質のDAニューロンの発火増加や線条体でのDA遊離を促進することにより、錐体外路症状を抑制すると考えられる。また、統合失調症では、前頭前野のDA活性が低下しており、陰性症状や認知障害を引き起こしていると考えられている。5-HT2受容体遮断により、DAの遊離が起こり、陰性症状が改善される。
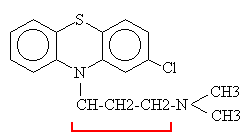
7、クロルプロマジン(chlorpromazine(CPZ))の薬理作用
活性基は、└─┘の部分にある。
薬理作用 | 解説 |
|---|---|
静穏作用 | 攻撃的な実験動物が取り扱いやすくなる。これは辺縁系のDAニューロンの抑制による。患者では妄想や幻覚症状が消える。自発運動の減少やいろいろな刺激に対する反応性が低下する。 |
条件回避反応の抑制 | この作用は、抗精神作用とよい相関を示すが、錐体外路症状をみている。 |
制吐作用 | 第4脳室底の化学受容器引き金帯(Chemoreceptor trigger zon、CTZ)に働き抑制する。CTZの血液脳関門(Blood brain barrier、BBB)が未発達であるため、BBBを越えないdomperidonにも制吐作用がある。 |
骨格筋の緊張低下作用 | 大脳基底核に働く。 |
体温低下作用 | 視床下部の体温調節中枢に働く。 |
催眠作用 | 静穏作用による。 |
鎮痒作用 | 抗ヒスタミン作用による。 |
プロラクチン分泌の亢進 | DA作用の抑制による。 |
自律神経系の抑制 | 各種神経伝達物質(DA、Norepi、5-HT、Histamine)の作用を抑制する。 |
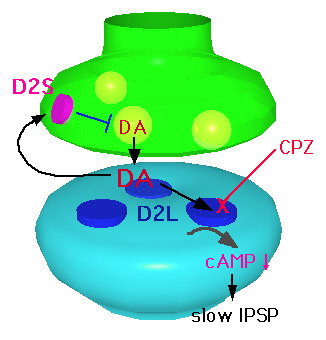
8、作用機作の模式図
DopamineシナプスとD2受容体 D2受容体には、D2SとD2L(第 3細胞内ループに29AAが挿入されている)の2種類が存在し、D2S受容体は主として前シナプス膜に存在し、autoreceptorとして働く。 |
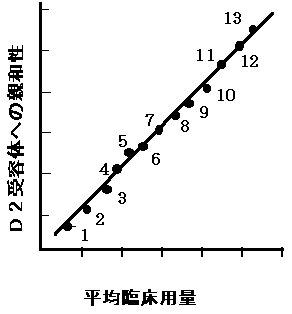
9、D2受容体への親和性と治療量との相関
1:spiroperidol | |
D2受容体遮断作用と臨床用量がよく相関する。また、D2受容体への親和性(遮断力)は、陽性症状の抑制と副作用についてはこのように綺麗に相関する。(P.Seeman,Biochem.Pharm,26,1741,1977) | |
10、クロルプロマジンの副作用
副作用 | 症状と解説 |
|---|---|
急性ジストニア(early dystonia) | 発症は投薬後1-5日。治療開始直後の頭頚部の運動障害、嚥下困難。抗コリン薬が効く。 |
アカシジア(akathisia) | 発症:5-6日後。じっと座っていられない(静座不能)。 |
錐体外路症状 | 発症:5-50日後。線条体のD2遮断による。 |
悪性症候群 | 発症:数日-数週後。高熱、骨格筋の硬直、昏迷、頻脈。ダントロレン(dantrolene)が治療薬(SRからのCa遊離抑制)。 |
遅発性ジスキネジア | 発症:数ヶ月後。20-25%に出現。増量で一時的に症状が改善するので、D2遮断により、受容体の感受性増加などにより、DA機能が代償的に増加するためと考えられている。非可逆性のことが多い。口周辺の不随運動(rabbit syndrome)。 |
起立性低血圧 | α1の遮断による。 |
皮膚過敏症 | 日光過敏症 |
肝障害 | 胆汁うっ滞 |
抗コリン作用 | 口渇、便秘、排尿障害 |
造血機能抑制 | 再生不良性貧血、溶血性貧血 |
生殖器 | FSHやLHの分泌抑制。排卵障害、不妊、不能をきたす。 |
痙攣閾値を低下 | てんかんの患者に注意。 |
体重増加 | 食欲亢進による。低力価薬で見られる。 |
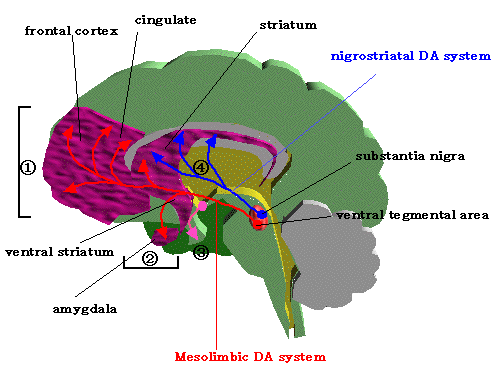
11、DAニューロンと統合失調症治療薬の作用および副作用発現
統合失調症治療薬は、1)の中脳皮質系DAと、2)の中脳辺縁系DAに働き、抗精神病作用と鎮静作用を示す。副作用の錐体外路症状は、4)の黒質線条体系のD2受容体の遮断により引き起こされる。prolactin分泌などの内分泌障害は、3)の視床下部・下垂体系DA遮断によりおこる。その他、中枢ヒスタミンおよびセロトニン受容体の遮断作用がある。また、末梢ムスカリン受容体遮断およびα1受容体遮断作用による副作用も生じる。 |
12、化学構造と薬理効果と副作用
第1世代薬(定型薬) | 薬物 | 受容体遮断 | 治療効果 | 錐体外路症状 | 鎮静作用 | 起立性低血圧 | 特徴、副作用など |
|---|---|---|---|---|---|---|---|
フェノチアジン系(Phenothiazines) | クロルプロマジン(chlorpromazine) | α1>D2 | 弱い | 中程度 | 強い | 強い |
|
フルフェナジン(fluphenazine) | D2>α1 | 強い | 強い | 弱い | 大変弱い | ||
イミノベンジル系(Iminodibenzyls) | カルピプラミン(carpipramine) | 5-HT>D2 | 弱い | 弱い | 弱い | 大変弱い | 意欲賦活作用。他の抗精神薬に付加。 |
ベンズアミド系(Benzamides) | スルピリド(sulpiride) | D2>>α1 | 弱い | 弱い | 弱い | 弱い | プロラクチン上昇、無月経の副作用 |
ブチロフェノン系(Butyrophenones) | ハロペリドール(haloperidol) | D2>α1 | 強い | 大変強い | 弱い | 大変弱い | 1%に悪性症候群 |
第2世代薬(非定型薬) | 薬物 | 受容体遮断 | 特徴、副作用など |
錐体外路症状や精神的副作用が少ない。共通する副作用として、体重増加、心電図QTc延長、性機能障害がある。 | |||
ジベンゾジアゼピン系(Dibenzodiazepines) | クロザピン(clozapine) | D4>5-HT2>D2 | 意欲賦活作用。agranulocytosis(0.8%)や心筋炎などの副作用。 |
複素環式化合物(Heterocyclic)系 | リスペリドン(risperidone) | 5-HT2>D2 | α1遮断による起立性低血圧。 |
ペロスピロン(perospirone) | 我国で開発。効果発現が速い。抗精神病作用は強い。 | ||
クエチアピン(quetiapine) | 抗コリン作用はほとんどなし。α1遮断による起立性低血圧。血糖値上昇のため、糖尿病患者に禁忌。効果発現が遅い。 | ||
オランザピン(olanzapine) | 副作用として血糖値上昇。糖尿病患者に禁忌(オランザピンが膵β細胞へ毒性を発揮、プロインスリンの成熟を妨げることが明らかになった、記事をみる)。 | ||
| ブロナンセリン(blonanserin) | D2>5-HT2 | 陽性および陰性症状に効果がある。 | |
キノリノン系(Quinolinones) | アリピプラゾール(aripiprazole) | シナプス後D2の弱い遮断作用とシナプス前D2(自己受容体)の刺激作用を併せ持つ。 | 陰性症状にも有効。プロラクチン(prolactin)亢進作用がない。錐体外路症状が少ない。体重増加やQTc延長はない。 |
ハロペリドール(haloperidol)
高力価の抗精神病薬であるが、運動障害が強い。抗コリン作用は弱い。他の高力価薬として、フルフェナジン(fluphenazine)とチオチキセン(thiothixene)がある。 |
リスペリドン(risperidone)
| 第2世代薬である。D2より5-HT2A受容体に対して 遮断作用が強いため、錐体外路系の副作用が少ないこと、陰性症状の改善作用を持つことなどが特徴である。最近は、ペロスピロン(perospirone)やオランザピン(olanzapine)が非定型薬として認可されている。 |
話題
150研究のメタアナリシスにより、第二世代の抗精神薬を、第一世代薬と有効性と副作用について、2万人の患者で比較した。4つの第二世代薬(有効順:clozapine>amisulpride>olanzapine>risperidone)が、第一世代よりも優れていた。他の第二世代薬は、第一世代よりも有効とはいえなかった。また、陰性症状の改善作用も第二世代薬の特徴ではなかった。錐体外路系の副作用は第二世代薬で少なかったが、鎮静作用や体重増加作用などは第二世代薬間でも差異がみられた。第二世代薬は、多くの性質が薬物間で異なっており、均質なクラスとはいえないので、個々の患者に合った治療をする必要がある。 (S.Leucht et al, Lancet, 373, 31,2009、論文をみる)
米国マサチュセッツ総合病院で、5つの精神疾患(autism spectrum disorder, attention deficit-hyperactivity disorder, bipolar disorder(BD), major depressive disorder and schizophrenia)の遺伝子(約3万3千人)のSNPsを調べ、4つのリスク遺伝子(Chr3上のITIH3、Chr12上のCACNA1C(Caチャンネル)、Chr10上のCACNB2(Caチャンネル)とNEURL)を見出した。CACNA1Cは、既報のようにBDとSchizoと強く関連していたが、他の3つの遺伝子は5つの精神疾患すべてと関連していた。これらの結果より、Caチャネル遺伝子活性の違いが、精神疾患の多様な症状を引き起こしている可能性があると示唆された。(J.W.Smoller et al, Lancet, 381, 1371, 2013、論文をみる)
統合失調症については、これまで「原因遺伝子を発見する」研究は数多く行われたが、どれも不発で、小さな遺伝的および孤発的な変異が数多く積み重なって発症するという、発症メカニズムの解明や治療に直結しない結果しか得られていなかった。本研究では、統合失調症全体の0.13%という極めて「稀」な場合に限られるけれども、SETD1Aという1つの遺伝子の機能異常が統合失調症に結びつくということが明らかにされた(Tarjinder Singh et al, Nature Neurosci. 19, 571, 2016、論文をみる)。
関連サイトの紹介
1、地域精神保健福祉機構 抗精神病薬 薬物療法 統合失調症・妄想性障害・緊張病
2、日本生物学的精神医学会誌 27(3):158─ 162, 2016 精神疾患のゲノム解析の現状と展望
(三木、久野)