血液凝固および貧血に関する薬物(Drugs Acting on Blood Coagulation and Anemia)
Anti-Thrombosis Agents (抗血栓症薬)は、病的な内皮の損傷(動脈硬化など)やその他の 原因による血栓形成促進状況(心房細動、人工弁)における血栓症、血栓栓塞症の治療や予防の ために使用される。血栓栓塞症(脳、心など)の急性期には、まず、線溶系の活性化薬 (Thrombolytics)、ついで速効性のHeparin、維持と予防に経口可能なWarfarinなどの Anticoagulantsが用いられる。また、動脈系の血栓形成自体には血小板凝集阻害薬 (Anti-Platelets)が用いられる。逆に、組織障害などによる出血とは血管外への血球成分の漏出と定義され、その程度にもよるが、自然に止血する。これを補助・促進するために止血薬(Hemostatics)がある。
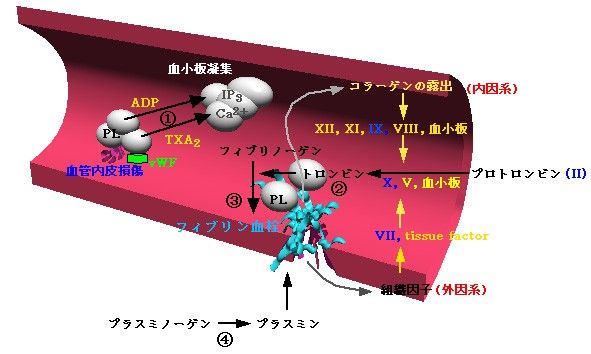
1、 止血・線溶機構
一次血栓形成: 血管内皮の損傷により露出したコラーゲンに、von Willebrand 因子(vWF)を介して血小板が付着し、活性化され(1)、ADPやTXA2の遊離、種々の接着蛋白質(フィブリノー ゲンなど)により血小板の凝集をもたらす。動脈では、血小板が主体となる白色血栓が生じる。この予防と治療には抗血小板薬が用いられる。 |
2、Antiplatelets(抗血小板薬)
抗血小板薬は、血小板に働いて血栓形成を抑制する。主に動脈硬化に伴う脳梗塞や心筋梗塞を予防する目的で使用されるが、これは血小板による血液凝固が主に血流の早い動脈で起きるためだと考えられている。一方、血流の遅い静脈や心房内で起きる血液凝固予防には抗凝固薬が用いられる。
日本での抗血小板薬の処方頻度を調べたところ、1位アスピリン(72.5%)、2位クロピドグレル(12.6%)、3位シロスタゾール(4.2%)であった(日経メディカルonlineによる、2019/3/30)。
分類 | 薬物 | 作用機序など |
|---|---|---|
シクロオキシゲナーゼ阻害 | アスピリン(aspirin) | トロンボキサンA2(TXA2)は、アラキドン酸代謝産物の1つで、活性化された血小板内でシクロオキシゲナーゼ(COX)により産生され、放出されたTXA2は血小板表面の受容体に結合し、Gタンパク質を介したシグナルにより血小板凝集を誘導する。アスピリンは、COX分子内のセリン残基のヒドロキシル基をアセチル化して不可逆的に阻害し、TXA2産生を抑制し、血小板凝集を阻害する。 核のない血小板ではCOXは再合成されないので、アスピリンの半減期は0.44時間と短いが、抗血小板作用は不可逆的で、血小板の寿命(7~10日)の間、凝集抑制効果が持続する。 一方、血管内内皮細胞内では、COXはアラキドン酸からプロスタサイクリン(PGI2)を合成する。PGI2はTXA2とは逆に血小板凝集を阻害する。アスピリンは、COXを抑制してPGI2産生も低下させるが、内皮細胞は核を持つのでCOXが再合成される。そのため、低用量のアスピリンは、血小板のTXA2は著明に低下させるが、PGI2はほとんど低下させない。しかし、高用量のアスピリンは、プロスタサイクリン産生も減して相反する効果が出現する。このことを「アスピリンジレンマ」という。 消化管出血のリスクが増加。長期の服用は大腸がんリスクを低下させる。 |
トロンボキサンA2合成 阻害 | オザグレル(ozagrel) | クモ膜下出血後などの脳循環障害に用いられる。 |
ADP受容体(P2Y12受容体)阻害薬 | チクロピジン(ticlopidine) | 活性化された血小板から放出されたアデノシン二リン酸(ADP)が、ADP受容体 (P2Y12受容体)に 結合すると, Gタンパク質を介してアデニル酸シクラーゼが抑制され,血小板内 cAMP レベルを低下し,細胞内カルシウム濃度を上昇することで血小板凝集が促進される。 これらの薬物は、P2Y12受容体に対して選択的、直接的な阻害作用を有し、ADPによるずり応力惹起血小板凝集(shear-induced Platelet aggregation、SIPA)を抑制する(アスピリンは抑制しない)。チクロピジンはプロドラッグ(prodrug)であり肝で代謝され活性化される。チクロピジンよりもクロピドグレルの方が副作用が少ない。プラスグレルは、クロピドグレルに比べより強力で効果発現が早いとされている。チクロピジン、クロピドグレル、プラスグレルは受容体に不可逆的に結合するが、チカグレロルは可逆的に結合するため、投与終了後には速やかに作用が消失する特徴がある。 消化性潰瘍のリスクはアスピリンよりも低い。 |
ホスホジエステラーゼ阻害 | ジピリダモール(dipyridamole) | 血小板内で大部分のcAMPの分解を司っているホスホジエステラーゼ3(PDE3)を特異的に阻害することにより、血小板内cAMPレベルを上昇させることで血小板の凝集を阻害する。 侵襲的処置が必要となった場合の休薬期間が短い。脳血管の拡張により頭痛がおこることがある。 |
5HT2受容体遮断 | サルポグレラート(sarpogrelate) | 慢性動脈閉塞症に(末梢循環改善)用いられる。 |
3、抗凝固薬(Anticoagulants)
心房細動(左心耳にできる静脈血栓)や深部静脈血栓症などに用いる。偶然発見されたヘパリンやワルファリンは画期的な治療薬で今でも抗血栓薬の主役を担っている。長年、唯一の経口抗凝固薬として使用されてきたワルファリンは作用発現の遅さ、抗凝固能のコントロールの難しさ、出血の副作用、他剤との相互作用など、臨床上多くの問題点を持つため、新しい機序の経口抗凝固薬が求められてきた。
X因子は内因系および外因系が合流する凝固カスケードの要であり、活性化X因子(Xa因子)はリン脂質上でプロトロンビナーゼ複合体を形成する。増幅されたトロンビンを阻害するより、その上流にあるX因子を阻害するほうが効率的である。新しい抗凝固薬を考えるときヘパリン(トロンビン、X因子阻害)→低分子ヘパリン(X因子阻害)→直接Xa因子阻害薬という流れに沿って理解するのがわかりやすい。
分類 | 薬物 | 作用機序など |
|---|---|---|
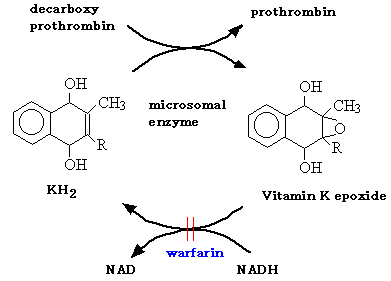
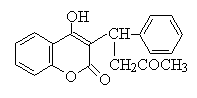
ビタミンK代謝拮抗 | ワルファリン(warfarin) | ビタミンK依存性凝固因子(プロトロンビン、VII、IX、X)の合成抑制。作用発現まで1-2日。経口可、血清アルブミン結合、代謝酵素誘導→薬物相互作用。過剰投与で出血傾向がでる。 |
| ヘパリン(heparin)
| ヘパリンは30-35Kで、アンチトロンビン(AT)IIIの作用増強(依存性)→セリン・プロテアーゼ不活性化。DIC、静脈血栓症、体外循環時に静注で投与する。過剰投与では、プロタミン(protamine)を投与する。 |
| 低分子ヘパリン | ダルテパリン(dalteparin) エノキサパリン(enoxaparin) フォンダパリヌクス(fondaparinux) | アンチトロンビンと結合するが、ヘパリンと異なりトロンビンとは結合できないことから、Xa因子への特異性が高く、出血傾向が少ない。従来から使用されてきたdalteparinやトロンビンに対しXa因子に4倍の特異性があるenoxaparin、ペンタサッカロイドのfondaparinux(Xa因子にほぼ特異的)が注射薬として静脈血栓塞栓症の予防薬に用いられる。 体外循環ができ、出血の副作用少なく、作用時間が2倍。 |
| 直接トロンビン阻害薬 | アルガトロバン(argatroban)(合成Arg誘導体) ダビガトラン(dabigatran) | アンチトロンビン非依存性に、 遊離のトロンビンだけでなく、フィブリン結合トロンビンを阻害。現在、argatroban(注射剤)の他、唯一の経口直接トロンビン阻害剤dabigatranが使用されている。dabigatranは食事や他の薬物の影響が少なく、INRの検査も必要がない点は、warfarinよりも優れている。心房細動患者の脳卒中発症予防の第一選択薬となっている。dabigatranのプロドラッグ体の吸収はP-糖蛋白質によって阻害されている。イトラコナゾール(itraconazole)などのアゾール系抗真菌薬やベラパミル(verapamil)などのP-糖蛋白質を強く阻害する医薬品を併用した場合、プロドラッグ体の吸収が亢進し、dabigatranの血中濃度が上昇することが報告されており,抗凝固作用が増強され、大出血を起こす可能性がある。イトラコナゾールの経口製剤は,特に強い阻害作用を示すため,dabigatranと併用禁忌となっている。 |
| 直接Xa因子阻害薬 | リバーロキサバン(rivaroxaban) アピキサバン(apixaban) エドキサバン(edoxaban) | アンチロンビン非依存性にプロトロンビナーゼ複合体内のXa因子を阻害。心房細動における虚血性脳卒中や全身性塞栓症の予防に用いられる。アンチトロンビンIIIの作用増強作用はほとんどな い。当初,新規経口抗凝固薬(novel oral anticoagulants:NOAC)と呼ばれたが,現在では直接経口抗凝固薬(direct oral anticoagulants:DOAC)と呼ばれることが多い。日本循環器学会の心房細動薬物治療のガイドラインが2013年に改訂され、これらのDOACが非弁膜性心房細動の第一選択薬となった。rivaroxabanの副作用として間質性肺炎に注意。 |
ビタミン Kとワルファリンの作用点 |
ワルファリン(warfarin)
4、血栓溶解薬(Thrombolytics)
分類 | 薬物 | 作用機序など |
|---|---|---|
プラスミノーゲン活性化因子 | ウロキナーゼ(urokinase、u-PA) | α2プラスミン・インヒ ビターによる抑制以上にプラスミンを産生して効果→出血しやすい。 |
組織プラスミノーゲン活性化因子(tissue-plasminogen activator、t-PA) | tisokinase(天然型)、 alteplase(遺伝子組換型)。フィブリンに結合し、血栓上で活性化される。続いてプラスミンが生成され、フィブリンが分解されて血栓が溶解される。alteplaseは急性脳梗塞の治療薬として注目されている。発症後4.5時間以内に投与すると、有意に症状が改善する。重篤な副作用は症候性頭蓋内 出血である。発症後9時間まで投与可能なdesmoteplaseが開発中である。 |
5、止血薬(Hemostatics)
分類 | 薬物 | 作用機序など |
|---|---|---|
血管強化薬 | カルバゾクロム(carbazochrome)、etamsylate、ビタミンC、フラボノイド類(柑橘) |
|
ビタミンK | フィロキノン(phytonadione、活性型) | ビタミンK依存性凝固因子(プロトロンビン、VII、IX、X)の合成(肝)に必要、か つ、合成を促進する。Glu 残基のγ‐カルボキシル化 :Ca結合warfarinに拮抗 |
凝固因子の補充(遺伝子組換体) | トロンビン、VIII、IX、XIII、vW因子など | 血友病や凝固促進に用いる。 |
抗線溶薬 | トラネキサム酸(tranexamic acid) | Lys類似体で、フィブリンのLys残基に競合し、プラスミンの結合を阻害する。 |
局所的作用薬 | トロンビン、 |
|
6、貧血治療薬(Antianemia)
貧血は、赤血球の数および血色素量の減少した状態で、多くの種類がある。大きく分けて3つに分類されている。貧血はヘモグロビン濃度の低下で判断される。男性はHb13g/dL未満、女性ではHb12g/dL未満 を貧血という。貧血は、1)赤血球の産生低下、2)赤血球破壊の亢進、3)失血、4) 血液の異常分布のいずれかで発生す る。これらを鑑別するために、MCV(平均赤血球容積)とMCHC(平均赤血球ヘモグロビン濃度)を求める。
| 小球性低色素性貧血 | 正球性正色素性貧血 | 大球性正色素性貧血 |
|---|---|---|
| MCV<=80、MCHC<=31 | MCV=81~100、MCHC=32~36 | MCV>=101、MCHC=32~36 |
| 代表例:鉄欠乏性貧血、その他:慢性感染症、炎症、 腫瘍、鉄芽球性貧血 | 代表例:溶血性貧血、再生不良性貧血、その他:腎性貧血、急性出血、内分泌疾患 | 代表例:巨赤芽球性貧血(VB12欠乏および葉酸欠乏による貧血)、その他:肝障害による貧血、網状赤血球増加 |
| 鉄欠乏性貧血は、全貧血の2/3を占める。出 血や摂取不足で鉄が不足するために生じる。女性は月経および 妊娠により鉄が失われるので、鉄欠乏性貧血が多い。治療薬:2価鉄化合物で、硫酸鉄、フマル酸鉄、グルコン酸鉄。貧血改善後も、貯蔵鉄の補充のために数ヶ月は継続投与する。副作用:悪心、嘔吐などの消化器症状 | 溶血性貧血の治療薬:ステロイドや免疫抑制薬 を用いる。腎性貧血の治療薬:erythropoietin | 巨赤芽球性貧血 は、 細胞分裂とDNA合成に必要なビタミンB12や葉酸が欠乏するために生じる。骨 髄像で特徴的な巨赤芽球が出現する。ビタミンB12の吸収には、胃の内因子が必要であるので、胃摘出後に巨赤芽球性貧血が見られる。 治療薬:VB12(cyanocobalamin)および葉酸 |
生体内 の鉄量は男性50mg/Kg、女性 35mg/Kgであり、その約65%は赤血球ヘモグロビンに存在する。約25%はフェリチンやヘモジデリンとして貯蔵されている。食事に含まれる鉄量は20~30mgで、このうち1~2mgが小腸から吸収され、鉄喪失量(男性:1mg/日、女性:1.5-2mg/日)とバランスを保っている。
話題
Thrombinは、fibrinogenを分解し fibrinを形成することはよく知られているが、血小板をも活性化する。血小板表面には、複数のPAR(protease-activated receptor)が存在する。PARのN末がthrombinにより切断されると、血小板の形態変化やADPの遊離、血小板の凝集が起こる。マウスには、PAR3とPAR4が存在し、PAR4をノックアウトすると、血小板の形態変化やADP遊離、細胞内Caの変化や凝集が起こらないことが明らかにされた。このことより、止血には、thrombinによる血小板の活性化が必要であることが明らかにされた。また、この過程を阻害する薬物の開発も期待される。 (G. R. Sambrano et al. Nature, 413, 74, 2001、論文をみる)
スエーデンのカロリンスカ大学で、t-PAの使用経験が十分ある施設と使用経験の少ない施設の合計285施設(比率1:1)からの急性脳梗塞患者約6500人について、alteplaseを投与後の症候性脳出血、3ヶ月後の死亡率、3ヶ月後の機能的自立率について調べた。1日目の症候性脳出血の割合は、両施設でほぼ同じで1.7%あった。7日目の症候性脳出血もほぼ同じで7.3%であった。3ヶ月後の死亡率は経験施設では約11%、未経験施設では13%であった。3ヶ月後の自立率は両施設で差はなく約50%であった。以上のことより、未経験の施設でもalteplaseをルーチンに有効に使用できることが示された。 (N. Wahlgren et al, Lancet, 369, 275, 2007、論文をみる)
ヒルジン(hirudin)という抗凝固薬があります。トロンビンの阻止薬です(補足:Bivalirudinはヒルジンの合成誘導体です)。ヒルジンは、ヒル(吸血虫)の唾液中から、発見、精製されました。日本では使用されていないですが、欧米では、血栓症の治療薬として実際使われています。ヒルジンやBivalirudinは、流血中のトロンビンのみならず、フィブリンに吸着したトロンビンも抑制するためにヘパリンよりも有効ではないかと言う期待がもたれています。ヒルが人間から血を吸っている時に、血が固まって、途中から血を吸えなくなったら、ヒルはショックですよね。そうならないように、ヒルの唾液からは血液を固まらせない(凝固させない)成分が出ているのです(金沢大学のサイトより)。
関連サイトの紹介
1、国立循環器病研究センター 循環器病情報サービス 血液をさらさらにする薬
2、同上 心房細動と付き合うには- 心原性脳塞栓症のリスクと新しい予防薬 -
3、イムス冨士見総合病院 tPA静注による超急性期血栓溶解療法
(佐伯)