脂質異常症治療薬(Drugs for Dyslipidemia)
1、脂質異常症とコレステロール
脂質異常症は、動脈硬化症の重要な危険因子であり、脳卒中や虚血性心疾患の発症に深く関係している。LDL-コレステロールやトリグリセライド(中性脂肪)が高く、HDL-コレステロールが低い場合に、動脈硬化が進行すると言われている。2007年4月に、日本動脈硬化学会は、動脈硬化のリスクとして、従来の総コレステロール(T-Chol)値を採用せず、その代わりにLDLコレステロール(LDL-Chol)値を採用することにした。また、高脂血症の変わりに、脂質異常症(dyslipidemia)を用いることにした。さらに、日本動脈硬化学会による脂質異常症の診断基準が2012年に改訂され、下の表のようになりました。
新しい診断基準では、「LDLコレステロールが多い場合」、「HDLコレステロールが少ない場合」、「中性脂肪が多い場合」という3つのタイプを明確にし、いずれも脂質異常であることをはっきりさせたといえます。肥満などが原因で高血圧や糖尿病などを併発している場合や、家族に心筋梗塞や狭心症などの病歴がある場合などには、リスクが高いと判断されます。この場合には、LDLコレステロール値を、リスクに応じて100~120mg/dl以下におさえるなど、治療目標が厳しくなる。
脂質異常症の診断基準(空腹時採血による数値)
| コレステロール | 数値 | |
|---|---|---|
高LDLコレステロール血症 | LDLコレステロール値 | 140㎎/dl以上 |
境界域高LDLコレステロール血症 | LDLコレステロール値 | 120~139㎎/dl以上 |
低HDLコレステロール血症 | HDLコレステロール値 | 40㎎/dl未満 |
高トリグリセライド(中性脂肪)血症 | トリグリセライド値 | 150㎎/dl以上 |
(日本動脈硬化学会「動脈硬化性疾患予防ガイドライン」2012年版より)
コレステロールの由来 | 一日量 | 組織での合成割合 |
|---|---|---|
食事から摂取 | 0.3-0.5g |
|
生体内で合成(内因性コレステロール) | 1-1.2g | 肝臓で50%合成、腸管で15%、皮膚で35% |
従って、内因性コレステロール合成を抑制する治療薬が必要とされる。
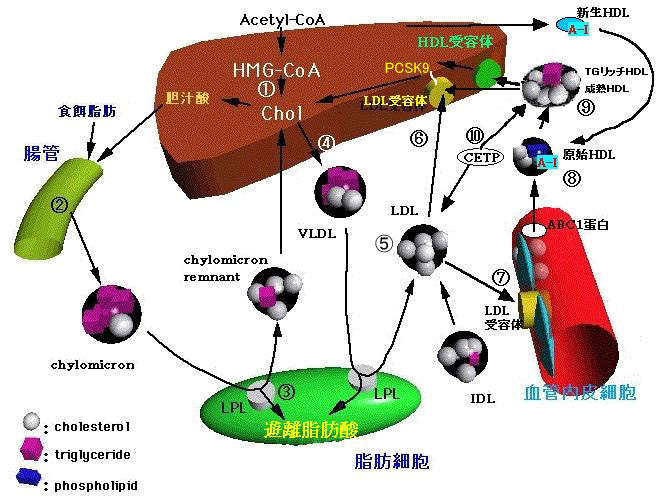
血漿リポ蛋白の種類と代謝 |
2、抗脂質異常症薬
分類 | 薬物 | 作用機作と副作用 |
|---|---|---|
1)コレステロール合成阻害 | プラバスタチン(pravastatin) | HMGCoA reductaseを阻害する、小腸と肝臓の酵素を選択的に阻害する。副作用は過敏症状、下痢、肝障害、横紋筋融解症、CPKの上昇、尿酸の上昇。pitavastatinは、CYPで代謝されない非代謝型スタチン。 |
| 2)PCSK9阻害薬 | エボロクマブ(evolocumab) | モノクローナル抗体で、LDL受容体に結合したPCSK9の機能を阻害し、LDL受容体の分解を抑制することにより、LDLの取り込みを促進する。家族性高コレステロール血症に用いる。皮下注射投与でスタチンと併用する。 |
3)コレステロール吸収阻害と代謝促進 | コレスチラミン(cholestyramine) | 陰イオン交換樹脂で、胆汁酸と吸着し、胆汁酸の再吸収を減少させる。このため、cholから胆汁酸合成経路が活性化され、血漿cholが減少する。副作用は胃腸障害、そう痒。 |
| 4)小腸コレステロールトランスポーター阻害薬 | エゼチミブ(ezetimibe) | 小腸上部の刷子縁膜に存在するコレステロール輸送体NPC1L1を特異的に阻害する。胆汁性と食事性のコレステロールの吸収を約50%抑える。副作用は胃腸障害。 |
5)血中リポタンパク分解促進、 リパーゼ活性化 | クロフィブラート(clofibrate) | LPL活性を増加させることにより、高TG血症に用いられる。標的分子はPPARαで、TG代謝に関わる遺伝子の転写を調節する。副作用は、横紋筋融解症が重要。肝障害もあるので、スタチンとの併用は推奨されない。副作用は下痢、めまい。 |
6)ニコチン酸 | ニコモル(nicomol) | 肝臓からのVLDL放出の抑制。副作用は発疹、顔面紅潮 |
7)その他 | プロブコール(probucol) | cholの胆汁中への異化排泄促進と、chol生合成の初期段階を抑制しLDL合成を抑える。高酸化作用がある。副作用は、心室性不整脈、QT延長症候群、消化器症状、発疹など。 |
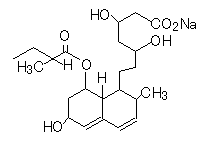
プラバスタチン(pravastatin)
話題
ヘルシンキ大学から、simvastatinを10年間投与した約2,000人の患者について、プラセボ群(最初5年間はプラセボ投与で、後半5年間をsimvastatin投与、約2,000人)との生存率の比較が報告された。10年間simvastatinを投与した群において、心血管疾患の死亡率が17%、冠血管疾患による死亡率が24%、発癌率12%低かった。(T.E.Strandberg et. al., Lancet, 364, 771, 2004、論文をみる)
カナダのMacMaster大学から、LDLコレステロール(LDL-C)の低下とDHLコレステロール(DHL-C)の上昇のどちらが心血管による死亡率と関連しているかについて、108研究(約30万人)のメタ解析結果が報告された。10mg/dlのLDL-C低下は、心血管死の罹患・死亡率を7~4%低下させたが、10mg/dlのHDL-C上昇はほとんど影響がなかった。以上のことより、心血管疾患治療で、LDL-Cの低下を重視すべきであることが支持された。(M.Briel et al, MBJ, Feb 16;338:b92, 2009、論文をみる)
英国の心疾患予防グループは、血管疾患リスクのある約2万人を2グループに分けて、一方はsimvastatin(40mg)を投与し、他方はプラセボで、約5年間追跡して、脳心血管疾患の発生率を調べた。投与群ではLDL-コレステロールが39mg/dL低下した。これと比例して、脳心血管疾患の罹患と死亡率もプラセボに比べて減少(23%)した。さらにsimvastatin投与を中止して5年間追跡したところ、脳心血管疾患の罹患と死亡率の減少は持続した。また、癌の罹患率はsimvastin投与グループで増加しなかった。これらの結果は、早期のスタチン治療の開始と長期間の投与が有効であることを示している。(Heart Protection Study Collaborative Group, Lancet, 378, 2013, 2011、論文をみる)
関連サイトの紹介
1、日本心臓財団 動脈硬化性疾患予防ガイドライン・エッセンス
2、女性の健康推進室 ヘルスケアラボ 女性および高齢者の脂質異常症
(三木、久野、向井)